

导语:奥希替尼耐药患者在停药后复用靶向药会快速复发,这个临床怪象困扰着多量肺癌患者。当人人还在基因突变中搜寻耐药元凶时,一项磋商却转向表不雅遗传的挂念密码,为破解TKI耐药困局撕开一皆全新裂口。
图源:CMT
奥希替尼耐药机制纷纷复杂,MUC1-C成为跨通路耐药挂念总开关
表皮孕育因子受体酪氨酸激酶扼制剂(EGFR-TKI)奥希替尼是EGFR突变非小细胞肺癌(NSCLC)的一线步调调养,但10-20个月内可现取得性耐药,其中约50%患者耐药机制不解,且即使针对MET扩增或C797S突变等已知耐药通路开发新一代扼制剂,患者仍会在散工夫内再次耐药。这种“闪电”复发情状领导,可能存在一种出奇基因突变的、可遗传的耐药挂念机制。既往磋商虽发现MUC1-C卵白在耐药捏续细胞中上调,并参与激活EGFR下流信号,但MUC1-C若何整合多态性耐药机制、若何编码可遗传的耐药挂念,也曾范畴内亟待破解的中枢贫瘠。更辣手的是,这种挂念是否通过表不雅遗传重塑杀青?是否存在可被药物靶向的挂念域?这些问题的谜底径直磋商到能否开发出广谱逆转TKI耐药的干与政策。
2025年10月,Signal Transduction and Targeted Therapy发表了一篇题为"MUCIN 1 confers inflammatory memory of tyrosine kinase inhibitor resistance in non-small cell lung cancer"的著作,该磋商独出机杼地锁定MUC1-C行为耐药挂念的分子“硬盘”,初度论说其通过STAT1-干扰素通路驱动炎症挂念,并在MUC1基因上发现两个增强子样挂念域,更关节的是考证了M1C抗体药物偶联物(ADC)可精确撤销耐药细胞,为破解TKI耐药这一生纪贫瘠提供了从机制到疗法的完满处理决议。

搭建耐药-停药-复敏-再耐药轮回模子,多组学层层解码MUC1-C挂念域功能
本磋商是一项整合细胞模子、动物本质与临床队伍的机制性蜕变磋商,旨在系统论说MUC1-C介导TKI耐药炎症挂念的分子机制及可干与性。磋商团队率先通过12周梯度递加奥希替尼浓度,从H1975细胞(EGFRL858R/T790M)中筛选出踏实耐药株H1975-OR(IC50达5.6 μM),模拟临床取得性耐药;继而斥地“药物假期”模子,将H1975-OR在无药培养基中传代12周,取得复敏株H1975-RT(IC50降至1.4 μM),精确模拟临床停药后复敏情状。为考证挂念效应,再将H1975-RT重新透露于奥希替尼,仅3周即重现耐药表型(H1975-RT-OR),酿成完满的耐药-复敏-再耐药闭环考证体系。
样本筛选严格罢黜功能依赖性原则:纳入MET扩增的患者着手MGH170细胞、佩戴EGFRT790M/C797S突变的MGH121细胞,隐敝主要耐药机制。本质分组收受遗传干与+药理学扼制双轨政策:通过doxycycline探究的shRNA系统敲低MUC1-C,使用GO-203多肽扼制剂阻断MUC1-C功能,并构建CRISPR-Cas9敲除株;同期斥地AFOS显性负性突变体阻断JUN/AP-1、PBRM1 shRNA干扰PBAF复合物等节点干与组。干与措施涵盖奥希替尼单药、奥希替尼勾通MET扼制剂(卡马替尼/萨沃替尼)、第四代TKI TQB3804,以及M1C ADC单药或勾通调养决议。主要评价标的包括:耐药挂念功能(IC50变化、克隆酿成才调)、表不雅遗传记号(ATAC-seq染色质可及性、ChIP-qPCR组卵白修饰)、转录组学特征(RNA-seq干扰素通路基因集富集)、卵白互作(染色质共千里淀)及临床磋商性(患者无发达生涯PFS、总生涯OS)。次要相当涵盖M1C ADC在PDX模子中的抗肿瘤活性与毒性。总计这个词谋划通过机制发现-功能考证-临床蜕变的递进逻辑,确保论断的因果严谨性与调养可操作性。
MUC1-C通过STAT1-干扰素双挂念域设立可遗传TKI耐药,靶向撤销使肿瘤负荷降75%
MUC1-C是TKI耐药炎症挂念的中枢驱动因子,而非单纯信号放大器
磋商团队率先通过剂量递加法设立奥希替尼耐药株H1975-OR,其IC50从亲代细胞的纳摩尔级飙升至5.6μM(图1a)。转录组对比分析揭示,耐药株中6860个基因上调,其中2838个基因在MUC1-C敲低后同步下调,huangguan体育app酿成耐药-挂念基因中枢集(图1d)。基因集富集分析(GSEA)自大,这些基因显赫富集于干扰素α/β信号通路和细胞畅达组织通路。功能考证中,将H1975-OR在无药培养基中净化12周取得复敏株H1975-RT,其IC50降至1.4μM,但染色质MUC1-C卵白水平仍显赫高于亲代细胞。更惊东说念主的是,重新透露于奥希替尼仅3周,H1975-RT便重获耐药(IC50=5.6μM),而敲低MUC1-C可竣工阻断该挂念性耐药再现(图2h)。在PC9细胞中过抒发MUC1-C雷同使耐药酿成工夫从12周裁减至2周(图2d)。
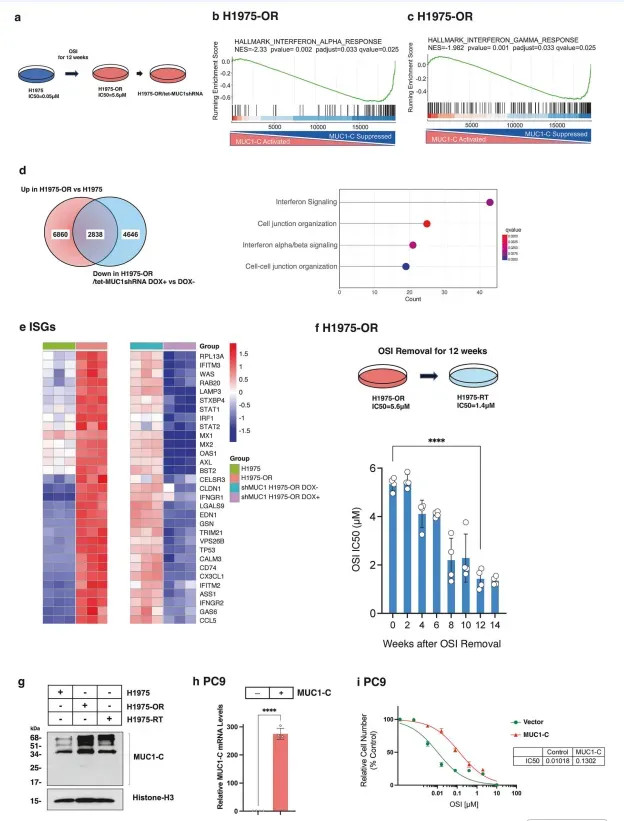
图1 MUC1-C依赖的炎症通路在奥希替尼耐药的H1975-OR细胞中相较于亲代H1975细胞的上调
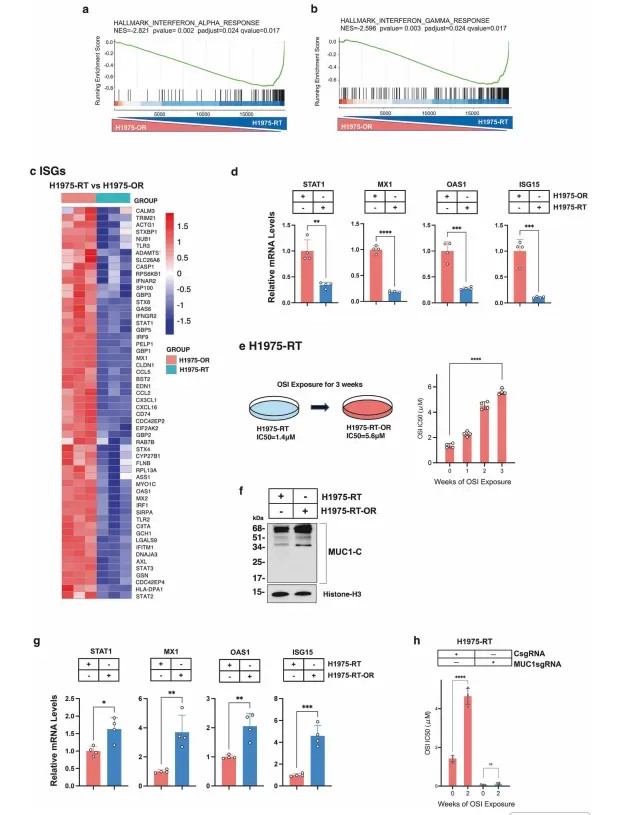
图2 H1975-RT细胞依赖MUC1-C激活奥希替尼耐药的挂念反应
STAT1-干扰素通路组成MUC1-C介导的挂念编码器,酿成自我强化正反馈环路
机制层面,奥希替尼刺激使H1975-RT细胞中MUC1-C mRNA在3天内激增30倍(亲代细胞仅4倍),同步激活STAT1转录(图3a)。染色质免疫千里淀(ChIP)确认,MUC1-C与STAT1共同占据MUC1基因上游的pELS-1挂念域(-541至-551 bp),富集度较未刺激组普及3-5倍(图3c)。敲低MUC1-C使STAT1对pELS-1的占有率下落60%以上(图3e),反之敲低STAT1也导致MUC1-C抒发诽谤70%(图3h),黄金城官网揭示二者酿成你中有我的自动调治环路。该环路下流,MX1、OAS1、ISG15等干扰素刺激基因抒发上调5-10倍(图1e),组成耐药挂念的效应模块。在患者着手的MGH170细胞(MET扩增型耐药)中,奥希替尼+萨沃替尼勾通调养反而使MUC1-C/STAT1轴激活更显赫,而MUC1-C扼制剂GO-203可将其逆转,评释注解该通路朝上耐药机制的普适性。
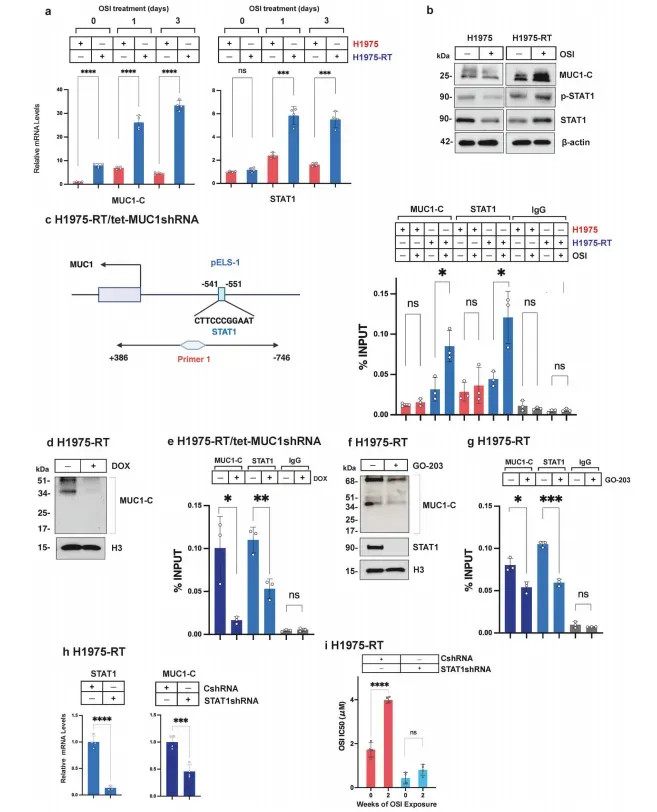
图3 MUC1通过STAT1介导的通路在奥希替尼调养的挂念反应中被探究
双挂念域单干妥协:pELS-1反馈即时刺激,pELS-2防守始终挂念
磋商初度浮滑MUC1基因存在两个功能特异的增强子样挂念域。pELS-1由STAT1驱动,崇敬快速最先;pELS-2(-1904至-1919 bp)则通过JUN/AP-1与PBAF复合物防守挂念捏久性。奥希替尼刺激下,pELS-2的MUC1-C、FOS、PBRM1占有率普及4-8倍,而JUN无明显勾通(图4b)。显性负性AFOS阻断JUN/AP-1后,pELS-2占有率下落75%,并竣工扼制耐药挂念酿成(图4f)。ATAC-seq自大,H1975-RT细胞pELS-1与pELS-2区域染色质可及性较胜代细胞增多2-3倍,敲低MUC1-C后可及性规复至基线水平。组卵白修饰分析揭示,pELS-2区域H3K27ac与H3K4me1千里积增多3-5倍,而扼制性修饰H3K4me3无变化,妥当活性增强子特征。
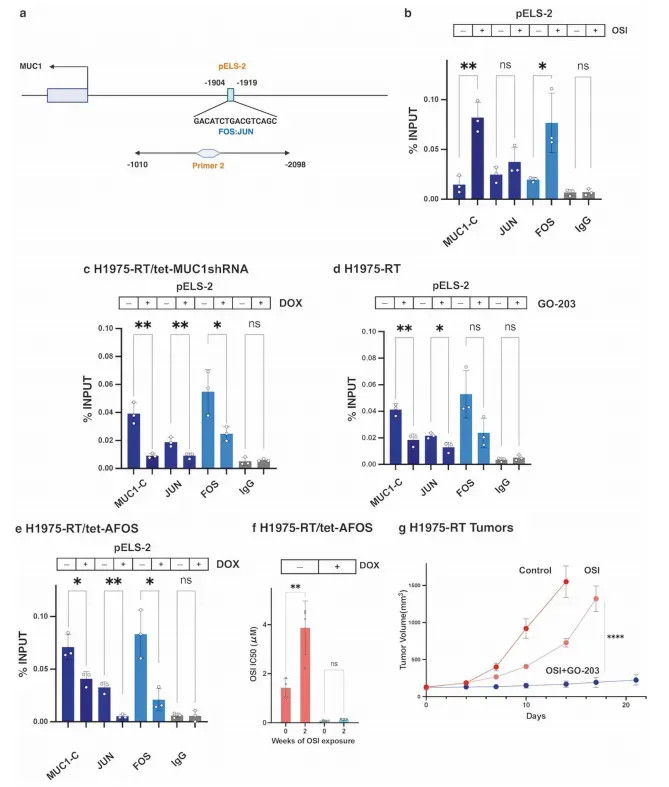
图4 在奥希替尼调养的炎症挂念反应中,MUC1-C的探究依赖于JUN/AP-1
PBAF复合物是挂念域结构骨架,M1C ADC可精确撤销耐药细胞
PBAF复合物组分PBRM1被确认是挂念域的结构胶水:其在pELS-1/2的占有率在耐药挂念中普及5-7倍,敲低PBRM1使MUC1-C抒发下落50%以上,并增强奥希替尼敏锐性(克隆存活率诽谤60%)。在动物模子中,H1975-RT移植瘤对奥希替尼竣工耐药(肿瘤体积增长至2000 mm³),而GO-203勾通调养使肿瘤缩小至500 mm³(图4g)。更具蜕变价值的是M1C ADC的疗效:在MET扩增的MGH170 PDX模子中,奥希替尼+萨沃替尼耐药后肿瘤捏续发达,M1C ADC单药调养3周使肿瘤体积从1000 mm³降至250 mm³,缩减75%,且小鼠体重踏实。体外本质自大,M1C ADC对H1975-OR、H1975-RT、MGH170、MGH121等耐药细胞的IC₅₀均在10-50 nM范围,与亲代细胞相当,评释注解耐药不收缩ADC疗效。
临床队伍考证MUC1-C/STAT1共抒发是独处预后记号物
对116例接管奥希替尼调养的EGFR突变NSCLC患者肿瘤样分内析,93.9%检测到MUC1-C抒发,其中37%为高抒发(Allred评分≥6)。高抒发组中位无发达生涯期(PFS)裁减至1.2年(低抒发组2.1年),疾病发达风险增多1.8倍(HR=1.83, 95%CI:1.25-2.67,P=0.0011);总生涯期(OS)雷同裁减(2.3年vs3.5年,P=0.0114)。多身分分析自大,MUC1-C高抒发是独处于TNM分期、脑搬动的预后因子(PFS:P=0.003; OS:P=0.008)。更关节的是,MUC1-C与STAT1抒发呈显赫正磋商(r=0.68,P<0.0001),双高抒发患者PFS进一步裁减至0.9年(图5)。
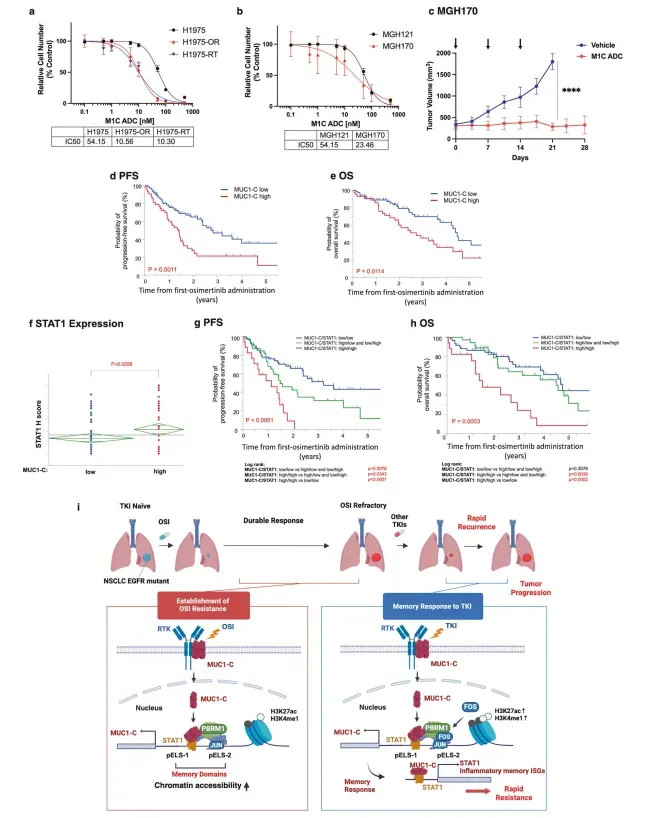
图5 MUC1-C在EGFR突变NSCLC中的抒发与对奥希替尼的
注:(a) 指定的NSCLC细胞系和(b)患者着手细胞用指定浓度的M1C抗体药物偶联物(ADC)处理7天,通过Alamar Blue染色分析细胞活力。为止(6次测定的均值±步调差)透露为相对细胞活力(%对照);(c) 荷瘤小鼠体内已设立的MGH170 PDX肿瘤在体积达到100 mm³时配对小鼠分为两组(每组6只),于指定日历尾静脉打针对照载体或M1C ADC(7.5 mg/kg)。(d) 无发达生涯期(PFS)和(e) 总生涯期(OS)的Kaplan-Meier弧线;(f) MUC1-C低抒发与高抒发水平与STAT1抒发的磋商性。(i) 暗示图态状MUC1-C驱动的炎症挂念反应导致NSCLC细胞对奥希替尼耐药;(i) pELS-1由MUC1-C和STAT1占据,以及(ii) pELS-2由MUC1-C、AP-1(JUN)和PBAF(BRG1、PBRM1)占据。反应磋商
回想
该磋商将TKI耐药见解化为可遗传的炎症挂念经过,其中枢孝敬在于揭示MUC1-C通过STAT1/AP-1/PBAF三轴驱动双挂念域表不雅重编程,突破耐药仅由基因突变驱动的传统知道。磋商设立耐药-复敏-再耐药完满功能周期模子,勾通ATAC-seq、ChIP-seq等多组学,将动态挂念经过拆解为可量化的染色质事件,号称靶向调养耐药磋商范式。蜕变层面,M1C ADC广谱撤销耐药细胞的疗效(肿瘤负荷降75%)与临床记号物考证(PFS裁减40%)无缝对接,为奥希替尼耐药后线调养提供首个东说念主源化精确疗法。磋商谋划的精妙之处在于,不仅发现机制,更通过PDX模子、患者生涯数据双重考证,使论断兼具科学深度与临床温度,径直鼓舞M1C ADC参加临床熟悉,为多量TKI耐药患者带来朝上耐药规模的切实但愿。
参考文件
Takamori S, Haratake N, Bhattacharya A, 等. MUCIN 1 confers inflammatory memory of tyrosine kinase inhibitor resistance in non-small cell lung cancer[J]. Signal Transduction and Targeted Therapy, 2025, 10: 389. DOI: 10.1038/s41392-025-02482-7.
“医学论坛网”发布医学范畴磋商恶果息争读HJC黄金城(GoldenCity)官网首页,供专科东说念主员科研参考,不行为诊疗步调,使用需把柄具体情况评估。
幸运飞艇APP官网下载